Cell: 不同白血病突变通过核相分离凝聚体驱动白血病发生
来源:BioArt 2025-11-29 09:17
该研究揭示了不同白血病突变如何通过核相分离凝聚体(C-body)这一共同机制驱动疾病发生,为白血病的治疗提供了新靶点。
蛋白质网络的空间组织是维持细胞功能有序性的核心机制,既依赖于膜结合细胞器的分区作用,也涉及核仁等无膜生物分子凝聚体的动态调控【1】。核磷蛋白(NPM1)作为核仁形成的关键因子,其定位异常往往反映细胞功能紊乱,并为研究癌症中蛋白质错误定位的致病机制提供了线索。在急性髓系白血病(AML)中,NPM1是最常见的突变基因之一,其突变体(NPM1c)因获得核输出信号而错误定位至胞质,却能异常驱动核内HOXA/MEIS1基因表达程序【2-4】。该程序亦见于其他AML亚型,且这些亚型对MENIN抑制剂等具有共同治疗敏感性,提示不同突变可能通过汇聚于同一致病机制促癌,但其具体关联及关键靶点仍有待阐明。
近日,来自美国贝勒医学院的Joshua A. Riback和Margaret A. Goodell研究团队合作在Cell杂志发表题为Disparate leukemia mutations converge on nuclear phase-separated condensates的研究论文。该研究揭示了不同白血病突变如何通过核相分离凝聚体(C-body)这一共同机制驱动疾病发生,为白血病的治疗提供了新靶点。

研究人员首先利用CRISPR基因编辑技术,在多种NPM1突变白血病细胞系和动物模型中对内源性NPM1蛋白进行荧光标记。通过活细胞成像等技术,他们首次清晰地观察到,突变型NPM1(NPM1c)在细胞核内形成了一种新型的、在生物物理性质上不同于核仁的生物分子凝聚体,并将其命名为“C-body”。重要的是,该结构在原发性患者样本中也得到证实。定量分析表明NPM1c在C-body中的富集度远高于胞质,且细胞周期追踪显示C-body在细胞分裂末期重新组装,并会延迟野生型NPM1(NPM1wt)的核输入,提示其具有动态性和功能主导性。
为了解析C-body的功能,研究人员通过免疫染色和生物物理分析,发现C-body中特异性富集了XPO1(核输出蛋白)、NUP98(核孔蛋白)、KMT2A(组蛋白甲基转移酶)和MENIN等关键调控蛋白,并与活跃的染色质标记共定位。CUT&RUN和DNA-FISH实验进一步证实,这些蛋白共同结合在白血病驱动基因(如HOXA簇和MEIS1)的位点上,直接将C-body与异常基因转录联系起来。功能获得和功能丧失实验证明,NPM1c对于C-body的形成及其对上述蛋白的招募既是必要的也是充分的。更重要的是,XPO1抑制剂可溶解C-body,而MENIN抑制剂则能导致MENIN从C-body中耗竭,两者均能有效抑制白血病基因表达并诱导细胞分化,在动物模型和患者原代细胞中均验证了这一效果。
研究人员通过截断突变体系统性地分析了NPM1c各个结构域的功能,发现其多价相互作用是驱动相分离形成C-body的基础。关键证据在于,只有在功能上能够形成C-body的NPM1c变体,才能在体外和小鼠体内维持细胞的未分化状态、驱动白血病相关基因表达并促进白血病发生;而无法形成C-body的变体则会导致细胞分化,失去致瘤能力。这直接证明了C-body的稳定性与白血病细胞的干性维持和增殖能力存在严格的因果关系,是维持恶性表型所必需的。
最后,研究将视野扩展到其他白血病亚型。他们发现由NUP98、KMT2A等基因的多种致癌融合蛋白自身也能在细胞核内形成凝聚体,并且这些凝聚体能够招募与NPM1c的C-body完全相同的蛋白网络(如XPO1、MENIN等)。通过相图分析等生物物理手段,证实这些由不同致癌因子驱动的凝聚体在本质上无法区分。
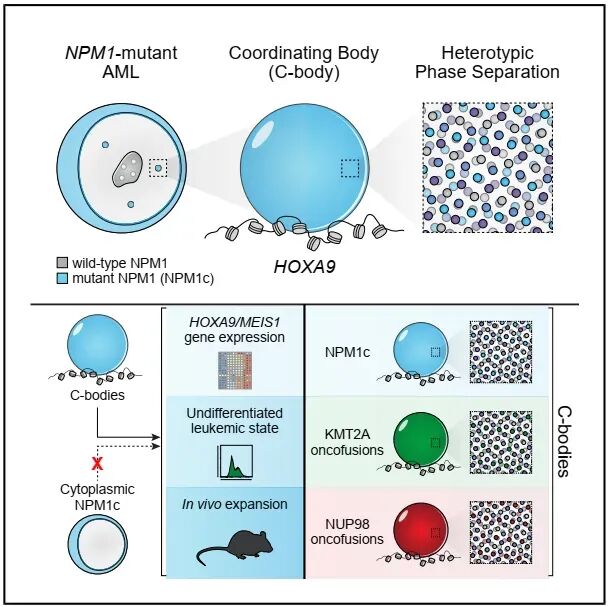
图一 不同白血病突变通过核相分离凝聚体驱动白血病发生
总之,这项工作发现,尽管基因突变的起点不同,但通过形成一种物理性质和作用机制相似的“C-body”来劫持关键的转录调控机器,是急性髓系白血病中一个跨亚型的、汇聚性的致病机制,为开发广谱靶向疗法提供了坚实的理论依据。
原文链接:
https://www.cell.com/cell/fulltext/S0092-8674(25)01149-3
参考文献
1. Lyon, A.S., Peeples, W.B., and Rosen, M.K. (2021). A framework for understanding the functions of biomolecular condensates across scales. Nat. Rev. Mol. Cell Biol. 22, 215–235.
2. Azmi, A.S., Uddin, M.H., and Mohammad, R.M. (2021). The nuclear export protein XPO1 — from biology to targeted therapy. Nat. Rev. Clin. Oncol. 18, 152–169.
3. Alcalay, M., Tiacci, E., Bergomas, R., Bigerna, B., Venturini, E., Minardi, S. P., Meani, N., Diverio, D., Bernard, L., Tizzoni, L., et al. (2005). Acute myeloid leukemia bearing cytoplasmic nucleophosmin (NPMc+ AML) shows a distinct gene expression profile characterized by up-regulation of genes involved in stem-cell maintenance. Blood 106, 899–902.
4. Brunetti, L., Gundry, M.C., Sorcini, D., Guzman, A.G., Huang, Y.H., Ramabadran, R., Gionfriddo, I., Mezzasoma, F., Milano, F., Nabet, B., et al. (2018). Mutant NPM1 Maintains the Leukemic State through HOX Expression. Cancer Cell 34, 499–512.e9.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


